記者9月29日從蘭州大學第一醫院(第一臨床醫學院)獲悉,該院、甘肅省生物治療與再生醫學重點實驗室李汛教授團隊取得重大科研突破——創新性提出“水凝膠+工程化外泌體”靶向治療策略,成功研發出水凝膠—干細胞外泌體遞送給藥體系,為肝纖維化逆轉開辟全新治療路徑。該項成果已發表于國際期刊《納米》。
肝纖維化是乙肝、丙肝、酒精性肝病、脂肪性肝病等慢性肝病的共同病理結果,若未及時干預,將逐步導致肝臟結構破壞、肝功能受損,最終發展為肝硬化甚至肝功能衰竭。據統計,全球每年約200萬人因肝臟疾病離世,其中近半數與肝硬化及其并發癥相關。
“在甘肅省,慢性肝病防治形勢尤為嚴峻:不僅慢性肝病患者基數大、乙肝丙肝流行周期長。”李汛表示,近年來,酒精性、脂肪性肝病負擔也持續加重,導致肝纖維化發病率居高不下。更關鍵的是,患者多集中在基層,現有治療手段有限,如何有效阻斷、逆轉肝纖維化,已成為全球醫學界的共同挑戰,更是我國及甘肅省公共衛生領域亟待解決的重點課題。
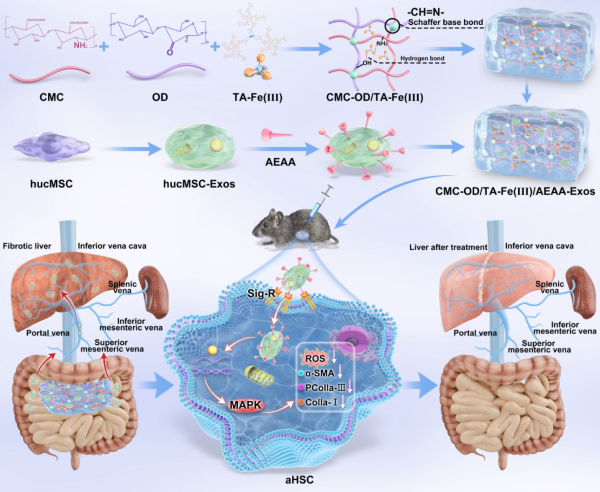
長期扎根西部的李汛教授課題組,構建了“臨床問題—基礎研究—臨床轉化”的完整科研閉環。針對肝纖維化治療痛點,團隊此次研究實現雙重創新:一方面,對具有修復再生、抗纖維化潛力的人臍帶間充質干細胞來源外泌體進行精準“改造”——通過氨基乙酰茴香酰胺修飾,讓外泌體獲得“導航能力”,可精準識別并靶向肝纖維化進程中的關鍵“元兇”——活化的肝星狀細胞,實現對病灶的“精準打擊”。另一方面,團隊將改造后的靶向外泌體裝載于可注射水凝膠中。這種水凝膠如同“藥物倉庫”,能在體內緩慢釋放外泌體,大幅延長其作用時間;通過腹腔注射方式,可將外泌體無損輸送至肝臟病灶,同步實現“持續釋放+精準靶向”的雙重治療效果。
實驗數據顯示,該水凝膠外泌體遞送體系安全性良好、療效顯著:細胞實驗中,改造后的外泌體可高效進入靶細胞,有效降低氧化應激、抑制膠原沉積;動物實驗中,該體系在肝臟的滯留時間延長至4周,能明顯減輕小鼠肝纖維化程度、降低炎癥反應,為臨床應用提供了扎實依據。
此次研究的核心突破,在于解決了外泌體在體內“半衰期短、靶向性差”的行業難題,不僅為慢性肝損傷、肝纖維化、肝硬化治療提供了全新思路,更具備極高的臨床轉化價值——目前該體系的制備工藝已申報發明專利。
李汛表示,下一步將加快推進成果的臨床前研究與臨床試驗,計劃依托現有平臺建立西北地區慢性肝病防治科研與轉化平臺,力爭將這一技術早日應用于肝纖維化、肝硬化及其他慢性肝臟疾病的臨床治療。
(受訪者供圖)
友情鏈接: 政府 高新園區合作媒體
Copyright 1999-2025 中國高新網chinahightech.com All Rights Reserved.京ICP備14033264號-5
電信與信息服務業務經營許可證060344號主辦單位:《中國高新技術產業導報》社有限責任公司